Inhaltsverzeichnis
37 Über das unterschiedliche Verhalten verschiedener Neutralisationsmittel hinsichtlich Intensität und Tiefenwirkung der Neutralisation aus dem Jahre 1963
Von H. Herfeld und I. Steinlein
About the different behaviour of diverse neutralising agents with regard to the intensity and the depth effect oft the neutralisation
After there has been reported on the necessary minimum intensity of the neutralisation of chrome leather in a previous publication, there „will be examined in the present essay the different neutralisation agents with regard to the maximum neutralisation obtainable, the danger of an excessive neutralisation and the depth effect. The test has proved characteristical differences between the various neutralisation agents relating thereto, thus enabling the expert to choose for each purpose the best neutralisation agent.
In der vorhergehenden Veröffentlichung berichteten wir darüber, welche Mindestneutralisation bei Chromleder erforderlich ist, um Säureschäden des Leders, Metallkorrosionen, Zerstörungen von Nähfäden und Hautreizungen bei Berührung mit der menschlichen Haut zu vermeiden. Wir konnten zeigen, dass der pH-Wert des wässrigen Auszuges von Chromleder zur Vermeidung dieser Nachteile auch unter ungünstigen Lagerbedingungen grundsätzlich nicht unter 3,5, in einigen Fällen, so beim Vernähen mit Baumwoll- und Leinenfäden und bei Berührung mit korrosionsempfindlichen Metallen und extrem feuchter Lagerung, nicht unter 4,0 liegen sollte. In der Praxis wird meist mehr oder weniger stärker neutralisiert, um eine tiefere Durchfärbung oder gleichmäßigere Fettverteilung zu erreichen und auch die Ledereigenschaften werden durch die Intensität der Neutralisation beeinflusst, worüber wir später noch berichten werden. Es hängt also von den jeweiligen Ledereigenschaften ab, welcher Neutralisationsgrad angestrebt wird. Bei vielen Lederarten reicht eine Neutralisation bis pH 4,5 aus, und eine stärkere Neutralisation wird tunlichst vermieden, da sie leicht zu gröberem Narbenbild und Losnarbigkeit führt. Bei anderen Lederarten werden etwas höhere pH-Werte angestrebt, keinesfalls aber über 5,5, da sonst mit den bekannten Gefahren einer Überneutralisation zu rechnen ist, die im Extremfall zu einer Sprengung der Gerbstoffhautsubstanzbindung und damit zu Entgerbungen führt. Damit ist der pH-Bereich, der für die Neutralisation zur Verfügung steht, abgegrenzt. Daneben spielt aber auch das pH-Gefälle innerhalb der einzelnen Schichten des Leders eine Rolle. Bei Ledern mit höherem Stand ist ein solches pH-Gefälle zwischen Innen- und Außenzone erwünscht, um insbesondere eine gleichmäßige Fettverteilung zu verhindern, bei weicheren Ledern wie Velour-, Bekleidungs und Handschuhleder wird dagegen eine möglichst gleichmäßige Durchneutralisation angestrebt, und auch bei Boxkalb und Rindbox wird heute zumeist ein wesentlich milderer Griff gefordert, als er vor Jahren für diese Lederarten noch üblich war.
Für die Auswahl der verschiedenen Neutralisationsmittel nach Art und Menge ist also wichtig zu wissen, wie sie sich vergleichsweise hinsichtlich der erreichbaren Neutralisationsintensität und der Gleichmäßigkeit der Durchneutralisation verhalten. Es ist bekannt, dass sich die einzelnen Neutralisationsmittel auch bei Anwendung äquivalenter Mengen und damit gleichen Alkaliverbrauchs in ihrer diesbezüglichen Wirkung auf das Leder stark unterscheiden. Hierzu liegen eine Reihe von Untersuchungen vor, vor einiger Zeit hat sich insbesondere Spahrkäs sehr eingehend mit dieser Frage befasst und unter Heranziehung von potentiometrischen Säuretitrationskurven, den Dissoziationskonstanten der verschiedenen Säuren, von Abstumpfungskurven und des bekannten unterschiedlichen komplexchemischen Verhaltens der einzelnen Anionen die verschiedenartige Wirkung der gebräuchlichsten Neutralisationsmittel hinsichtlich Intensität der Neutralisation und Tiefenwirkung diskutiert. Es sei auf diese für den Praktiker sehr aufschlussreichen Darlegungen verwiesen, die hier nicht nochmals wiederholt, sondern lediglich durch neuere Angaben ergänzt werden sollen.
Es fehlen nämlich bisher klare Angaben darüber, welche effektiven pH-Werte mit den einzelnen Neutralisationsmitteln unter verschiedenen Mengen- und Zeitbedingungen erhalten werden und überhaupt erreicht werden können, und wie sich die pH-Werte der Innen- und Außenzone effektiv unterscheiden. Spahrkäs hat zwar diesbezügliche Versuche erwähnt, bei denen bei Soda und Borax nach einer Woche noch kein Gleichgewichtszustand eingetreten war, und bei Natriumbikarbonat nach 3, bei Ammoniumbikarbonat nach 2 Tagen, bei Natriumsulfit und Acetat nach knapp einem halben Tag und bei Calciumformiat nach wenigen Stunden ein pH-Gleichgewicht erreicht wurde, wobei unter dem Begriff des Gleichgewichtszustandes sicherlich nicht unbedingt eine gleichmäßige Durchneutralisation in der ganzen Dicke zum Ausdruck gebracht werden sollte. Die gemachten Angaben enthalten aber keine konkreten pH-Angaben, sie sollten nur die großen Unterschiede in der relativen Geschwindigkeit des Entsäuerungsprozesses veranschaulichen. Häufige Anfragen aus der Praxis zeigen aber, dass insbesondere bei kräftigeren Chromlederarten (z. B. bei vielen technischen Ledern) Vorstellungen darüber fehlen, mit welchen Mitteln zur Erreichung eines bestimmten Neutralisationsgrades und einer bestimmten Durchneutralisation gearbeitet werden muss, und wie dabei Mengen-und Zeitfaktor einzustellen sind, wobei auch im Extremfall Neutralisationszeiten über 24 Stunden hinaus aus betrieblichen Gründen meist abgelehnt werden.
Den durchzuführenden Untersuchungen war demgemäß die Aufgabe gestellt, die verschiedenen Neutralisationsmittel hinsichtlich effektiver Neutralisationseffekte und Gleichmäßigkeit der Neutralisation in den einzelnen Lederschichten zu untersuchen. Dabei wurde von einem einheitlich hergestellten Chromleder ausgegangen, das aus feststrukturierten Rindkernstücken hergestellt Wurde und sehr kräftig gehalten war, um bei Schichtanalysen die unterschiedliche Tiefenwirkung in den einzelnen Schichten zuverlässig erfassen zu können. Das Hautmaterial wurde nach den üblichen Wasserwerkstattarbeiten und völligem Entkalken mit 100% Wasser, l% Schwefelsäure und 5% Kochsalz gepickelt und unmaskiert gegerbt, da Maskierungsmittel schon eine gewisse Vorneutralisation bewirken können. Verwendet wurden 2,5% Chromoxyd in Form von Chromosal B, wobei ein Drittel bei 33%, der Rest bei 45% Basizität zur Anwendung kam. Nach beendeter Gerbung lagerten die Leder 48 Stunden auf dem Bock und wurden dann durch Spalten egalisiert, um auch hinsichtlich der Stärke einheitliche Neutralisationsbedingungen zu schaffen. Die Stärke der Leder lag im feuchten Zustand bei 5,0-5,2 mm, im trockenen Zustand im Mittel bei 4,4 mm. Alle Mengenangaben über die Durchführung der anschließenden Neutralisationsversuche beziehen sich in Prozent auf das Spaltgewicht.
Die Kernstücke wurden in Stücke von 10 X 10 cm aufgeteilt und für jeden Versuch 7 Stück so über die Fläche verteilt, dass auf jeden Versuch ein etwa gleichartiges Hautmaterial kam, und strukturelle Unterschiede weitgehend ausgeschaltet wurden. Die Leder wurden dann V2 Stunde mit Wasser von 35 °C gespült und mit 200% Wasser von 35 °C und den berechneten Mengen an Neutralisationsmittel bei einer Zeitspanne von 2 und 24 Stunden neutralisiert, wobei die pH-Werte der Flotte am Anfang und Ende festgestellt wurden. Sie wurden dann wieder 1U Stunde bei 50 °C gespült, 45 Minuten bei 60 °C mit 100%. Wasser und 2% Avirol HL gelickert, leicht aufgespannt und bei Zimmertemperatur getrocknet. Der Chromoxydgehalt der Leder schwankte zwischen 4,1 und 4,3%, der Fettgehalt zwischen 0,8 und 1,2%. Dann wurde der pH-Wert des wässrigen Auszuges
sowohl am ungespaltenen Leder wie nach Spalten in 3 etwa gleich dicke Schichten bestimmt.
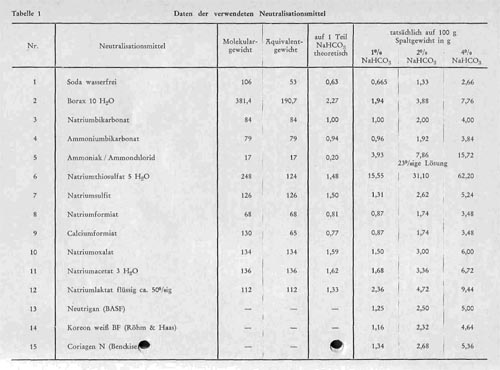
Tabelle 1:
Die Angaben über die verwendeten Neutralisationsmittel sind aus Tabelle 1 ersichtlich. Verwendet wurden 1, 2 und 4% Natriumbikarbonat auf Spaltgewicht, und die anderen Neutralisationsmittel wurden in „äquivalenten“ Mengen eingesetzt. Dabei wurden die Äquivalenzmengen durch potentiometrische Titration der Neutralisationsmittel mit Schwefelsäure auf pH 2,0 ermittelt, um auf diese Weise eine exakte Vergleichsbasis des Einsatzes zu finden und auch Neutralisationsmittel mit Firmenbezeichnung (Neutrigan, Koreon, Coriagen N) unter gleichen Äquivalenzbedingungen einsetzen zu können. Es wurden also stets diejenigen Mengen verwendet, die eine praktisch gleichartige Neutralisation von Schwefelsäure zu erreichen gestatten. Tabelle 1 gibt die Molekular- und Äquivalentgewichte der einzelnen Mittel an und außerdem die Mengen, die sich theoretisch aus den Äquivalentgewichten, auf 1 Teil Natriumbikarbonat bezogen ergeben. Dabei sei erwähnt, dass im Falle des Natriumsulfits, obwohl es sich hierbei.um ein 2wertiges Anion handelt, das Äquivalentgewicht gleich dem Molekulargewicht angegeben wurde, da schon Spahrkäs darauf hingewiesen hatte, dass nur die 2, Dissoziationsstufe der schwefeligen Säure mit einer Konstante von 1,0 x 10-7 derjenigen einer schwachen Säure entspricht, während die andere Dissoziationskonstante mit 1,5 x 10-2 derjenigen einer starken Säure entspricht (etwa der 2. Dissoziationskonstante der Schwefelsäure) und daher für eine Neutralisierungswirkung nicht in Betracht kommt. Das gleiche gilt auch für Natriumoxalat, da auch hier nur die 2. Dissoziationskonstante mit 6,4 x 10-5 einer schwächeren Säure, die 1. Dissoziationskonstante mit 5,9 x 10-2 dagegen einer starken Säure entspricht, so dass auch bei Natriumoxalat Molekulargewicht gleich Äquivalentgewicht angenommen wurde.
Tabelle 1 zeigt, dass die auf Grund der Titrationsergebnisse tatsächlich eingesetzten Mengen bei den meisten Neutralisationsmitteln den theoretischen Mengen etwa entsprechen. Geringfügige Abweichungen hängen mit dem jeweiligen Reinheitsgrad des Neutralisationsmittels, mit Verwitterungserscheinungen bei Borax oder im Falle des Natriumlaktats damit zusammen, dass es sich hierbei um eine etwa fünfzigprozentige flüssige Ware handelt.
Es muss indessen auf zwei Sonderfälle hingewiesen werden. Einmal wurde im Falle des Natriumthiosulfats eine etwa zehnfach größere Menge eingesetzt, als dem theoretischen Äquivalent entspricht. Spahrkäs hatte darauf hingewiesen, dass der rasche Abfall im Verlauf der Titrationskurve des Natriumthiosulfits, d. h. das Fehlen jeder Pufferung im pH-Bereich von 6 - 3 auf der Bildung der sehr starken Thioschwefelsäure (Dissoziationskonstante 4,5 x 10-1 bzw. 5,7 x 10-2) beruhe, die als solche daher für die Neutralisation nicht in Betracht kommt, anschließend aber einen allmählichen und sehr komplizierten Zerfall erleidet. Er folgerte daraus, dass es nicht möglich sei, Chromleder mit Thiosulfit nennenswert zu entsäuern, und dass der in der Praxis anzutreffende Einsatz von Thiosulfat mehr auf eine bleichende als auf eine entsäuernde Wirkung zurückzuführen sei. Das steht im Gegensatz zu Angaben von Stiasny und Prakke, die die komplizierten Zerfallserscheinungen der Thioschwefelsäure in schwefelige Säure und Schwefel oder in Polythionate, die für die neutralisierende Wirkung maßgebend sind, eingehend untersuchten und Thiosulfat zur Neutralisation von Chromleder besonders empfahlen, da eine Überneutralisation hierbei nicht zu befürchten sei. Sie führen dabei aber wiederholt an, dass ein erheblicher Überschuss und eine höhere Konzentration des Thiosulfats anzuwenden sei, da dadurch das Gleichgewicht der Zerfallreaktionen in die Richtung eines Verbrauchs an Wasserstoffionen verschoben würde, und dass bei zehnfach höherer Thiosulfatkonzentration schon eine zehnfach geringere Wasserstoffionen-Konzentration genüge, um die für die Neutralisation entscheidende Zersetzung zu erreichen. Außerdem brauchen diese Zerfallreaktionen Zeit, die Thiosulfatzerlegung verlaufe bei pH 1,6 rasch, bei 3,0 wesentlich langsamer, bei 4,0 nur noch sehr gering und bei pH 5,0 höre sie praktisch überhaupt auf. Es ist also verständlich, dass bei kurzfristig durchgeführten Titrationen diese für die Neutralisation entscheidenden Zerfallsreaktionen nicht erfasst werden. Unsere Titrationen, bei denen wir gleichzeitig durch zwischenzeitliches Erhitzen die Zerfallsreaktionen beschleunigten, haben als „Neutralisationsäquivalent„ die in Tabelle 1 angegebene wesentlich höhere Einsatzmenge für Thiosulfat ergeben, die in dieser Höhe für die Verwendung in der Praxis nicht in Betracht kommen dürfte. Trotzdem haben wir Neutralisationsversuche mit diesen Mengen durchgeführt, um die Widersprüche zwischen den Angaben von Spahrkäs und von Stiasny und Prakke zu klären.
Die andere Ausnahme ist die des Ammoniak-Ammonchlorid-Puffergemischs, bei dem das Ammoniumchlorid stets mit 5fl/o auf Spaltgewicht verwendet und die Ammoniakmenge entsprechend variiert wurde. Es handelt sich hierbei um ein stark gepuffertes System, so dass verständlicherweise auch hier bei den Neutralisationskurven höhere Ammoniakwerte ermittelt wurden, als den theoretischen Äquivalenzverhältnissen entspricht. Wir haben auch in diesem Falle die aus den Titrationen sich ergebenden höheren Mengen zur Anwendung gebracht und werden an späterer Stelle auf diese Frage nochmals eingehen.
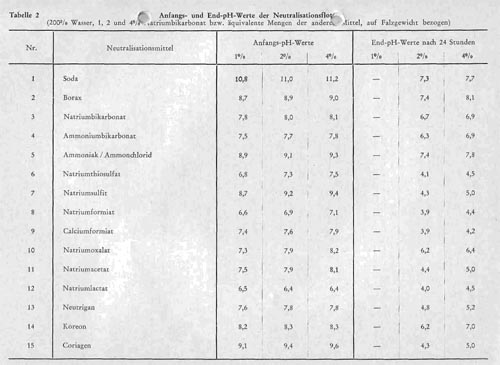
Tabelle 2:
In Tabelle 2 sind die Anfangs-pH-Werte der verschiedenen Neutralisationsflotten angegeben, und zwar jeweils bei 1%, 2% und 4% Natriumbikarbonat und den entsprechenden aus Tabelle 1 sich ergebenden tatsächlich eingesetzten Mengen der anderen Neutralisationsmittel. Ebenso enthält die gleiche Tabelle die End-pH-Werte der Lösungen bei 24-stündiger Neutralisationsdauer. Die Zahlen zeigen die starken Unterschiede, die zwischen den verschiedenen Neutralisationsmitteln hinsichtlich der Anfangs-pH-Werte wie der End-pH-Werte bestehen. Sie lassen damit bereits gewisse Schlüsse über den mit den einzelnen Neutralisationsmitteln erreichbaren Neutralisationsgrad zu, da die pH-Werte der neutralisierten Leder meist niedriger, keinesfalls aber höher liegen als die End-pH-Werte der Neutralisationsflotten. Daher sind insbesondere die End-pH-Werte bei hohen Ansatzmengen von Interesse, da sie Anhaltspunkte dafür geben, welche maximale Neutralisation mit den verschiedenen Neutralisationsmitteln erreicht werden kann, wobei niedere End-pH-Werte der Flotten zugleich auch auf eine starke Schonung des Narbens hindeuten. Nach dieser Richtung hin sind zwei Gruppen an Neutralisationsmitteln zu unterscheiden. Gruppe 1 umfasst Soda, Borax, Natriumbikarbonat, Ammoniumbikarbonat, Koreon und das Ammoniak-Ammoniumchlorid-Puffergemisch. Bei diesen sechs Produkten liegen die End-pH-Werte nach 24 Stunden bei Anwendung von 2% (die Prozentzahl in Äquivalenz auf Natriumbikarbonat berechnet) zwischen 6,2 und 7,4, bei Anwendug von 4% zwischen 6,9 und 8,1. Aus diesen hohen Werten ist bereits zu folgern, dass mit den Mitteln dieser Gruppe eine sehr intensive Neutralisation erreicht werden kann, dass aber mit der Anwendung höherer Mengen auch die Gefahr einer Überneutralisation verbunden ist. Das gilt in erster Linie für Soda, Borax und das Ammoniak-Ammoniumchlorid-Puffergemisch, in vermindertem Umfange aber bei höheren Einsätzen auch für Natriumbikarbonat, Ammoniumbikarbonat und Koreon. Dem steht eine 2. Gruppe von Neutralisationsmitteln gegenüber, bei denen selbst bei höchsten Einsatzmengen die End-pH-Werte der Lösungen etwa zwischen 4 und 5 liegen. Hierhin gehören einmal Natriumthiosulfat, Natriumformiat, Calciumformiat und Natriumlaktat mit End-pH-Werten zwischen 4,0 und 4,5 und ferner Natriumsulfit, Natriumacetat, Neutrigan und Coriagen mit End-pH-Werten bei Einsatz extrem großer Mengen zwischen 4,5 und 5,0, so dass selbst bei höchstem Einsatz dieser Mittel nicht mit der Gefahr einer Überneutralisation zu rechnen ist, aber auch der maximal erreichbaren Intensität der Neutralisation Grenzen gesetzt sind. Natriumoxalat mit einem maximalen End-pH-Wert der Flotte von 6,4 nähert sich schon dem Verhalten der Produkte der ersten Gruppe.
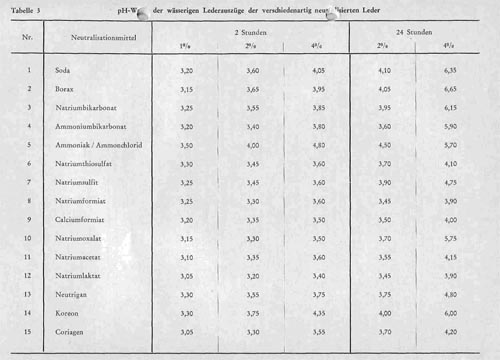
Tabelle 3:
Tabelle 3 gibt die in den wässrigen Auszügen der Gesamtleder zunächst ohne Rücksichtnahme schichtenmäßiger Unterschiede erhaltenen pH-Werte wieder. Die Zahlen bestätigen und erweitern die Folgerungen, die im vorhergehenden Abschnitt aus den pH-Werten der Restlösung gezogen werden konnten. Sie zeigen, dass bei einem so kräftigen Leder, unabhängig von der angewandten Menge des Neutralisationsmittels, die Zeit von 2 Stunden nicht ausreicht, um selbst mit 4!% Neutralisationsmittel eine Überneutralisation zu erreichen. In diesen Fällen liegen die pH-Werte meist noch verhältnismäßig dicht beieinander in einem pH-Bereich von 3,5-4,0. Sie ziehen sich dagegen weit auseinander, wenn man die Neutralisationsmenge genügend groß hält (4%) und gleichzeitig die Zeitdauer auf 24 Stunden erhöht. In diesem Fall ergibt sich auch wieder die gleiche Gruppenbildung, die wir oben mitgeteilt haben. Bei den Mitteln der Gruppe 1 liegen die pH-Werte der Leder bei Anwendung von 4'% und 24stündiger Neutralisationsdauer zwischen 5,70 und 6,65, wobei insbesondere im Falle von Soda und Borax schon der Gesamt-pH-Wert auf das Vorhandensein einer Überneutralisation mit allen Nachteilen hindeutet. Für die Gruppe 2 dagegen liegen die pH-Werte zwischen 3,9 und 4,8, zeigen also, dass trotz hoher Menge und Verlängerung der Neutralisationsdauer eine Überneutralisation auf keinen Fall zu befürchten ist, andererseits aber auch die erreichbare Neutralisationsintensität zwar für viele Lederarten genügt, aber in denjenigen Fällen, in denen eine besonders intensive Neutralisation erreicht werden soll, nicht ausreicht. Man wird vielleicht bei so kräftigen Ledern durch eine weitere Verlängerung der Einwirkungsdauer auch bei diesen Neutralisationsmitteln noch eine weitergehende Neutralisation erreichen können, sie wird aber niemals höher liegen können, als den oben angeführten End-pH-Werten der Lösungen entspricht. Eine gewisse Sonderstellung nimmt auch hier wieder Natriumoxalat ein, das eine höhere Intensität der Neutralisation als das Mittel der Gruppe 2 zu ergeben vermag, dagegen noch nicht die hohen Neutralisationswerte der Mittel der 1. Gruppe erreicht.
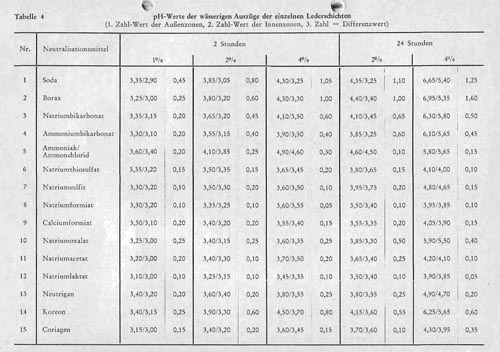
Nun sind die pH-Werte der wässrigen Auszüge der Gesamtleder nur mit Vorsicht auszuwerten, da sie Mischwerte darstellen, die keine Angaben darüber zu erhalten gestatten, wie die Neutralisation in den einzelnen Schichten des Leders erfolgt. Dieser letztere Faktor ist aber für die vergleichende Beurteilung der Neutralisationsmittel oft von entscheidender Bedeutung, und in Tabelle 4 werden daher die pH-Werte wiedergegeben, die bei den Schichtanalysen erhalten wurden, wobei jeweils die ersten Zahlen die mittleren pH-Werte der Außenzonen, die zweiten Zahlen die pH-Werte der Innenzone und die dritten Zahlen die Differenzwerte, d. h. die pH-Differenzen zwischen Außen- und Innenzone angeben. Hier machen sich die verschiedenen Unterschiede sehr deutlich bemerkbar, wobei insbesondere für die beiden Gruppen, wie die nachfolgende Gegenüberstellung zeigt, die Differenzwerte in weiten Grenzen variieren.
| Gruppe 1 | Gruppe 2 | ||
| 1% | 2 Stunden | 0,20 - 0,45 | 0,10 - 0,20 |
| 2% | 2 Stunden | 0,40 - 0,80 | 0,10 - 0,20 |
| 4% | 2 Stunden | 0,40 - 1,05 | 0,05 - 0,25 |
| 2% | 24 Stunden | 0,60 - 1,10 | 0,10 - 0,25 |
| 4% | 24 Stunden | 0,45 - 1,60 | 0,05 - 0,35 |
Tabelle 4:
Die Neutralisationsmittel der 2. Gruppe ergeben durchweg eine sehr gleichmäßige Neutralisation, nennenswerte Unterschiede zwischen Außenzone und Innenzone sind praktisch in keinem Stadium der Neutralisation, gleichgültig welche Mengen eingesetzt werden und wie lange die Einwirkungsdauer gewählt wird, vorhanden. Wesentlich ungünstiger verhalten sich die Neutralisationsmittel der Gruppe 1, die höhere Differenzwerte zeigen, wobei untereinander noch sehr starke Unterschiede vorhanden sind. Wichtig erscheint dabei auch die Feststellung, dass das pH-Gefälle sich bei den Mitteln dieser Gruppe mit zunehmender Neutralisationsdauer nicht verringert, eher noch etwas erhöht. Die diesbezüglich ungünstigsten Neutralisationsmittel sind in Übereinstimmung mit den Erfahrungen der Praxis Soda und Borax, wobei bei genügend langer Einwirkungsdauer und hohen Einsätzen des Neutralisationsmittels Borax noch ungünstiger als die Soda zu bewerten ist. Natriumbikarbonat und Ammoniumbikarbonat geben zwar eine gleichmäßigere Neutralisation, wobei die Unterschiede insbesondere bei hohen Einsätzen und längerer Einwirkungsdauer besonders deutlich werden, doch ist die Gleichmäßigkeit noch erheblich ungünstiger als bei den Produkten der Gruppe 2. Koreon ist ähnlich wie die Bikarbonate zu werten, und ebenso ist das Oxalat bei längerer Einwirkungsdauer mehr der Gruppe 1 als der Gruppe 2 zuzuschreiben. Eine Ausnahmestellung nimmt das Ammoniak-Ammoniumchlorid-Puffergemisch ein, das zwar eine intensive Neutralisation bewirken kann, wenn hohe Mengen eingesetzt werden und bezüglich der Gefahr einer Überneutralisation durchweg der Gruppe 1 zuzuordnen ist, sich aber von den übrigen Neutralisationsmitteln dieser Gruppe dadurch unterscheidet, dass es eine sehr gleichmäßige Durchneutralisation ergibt.
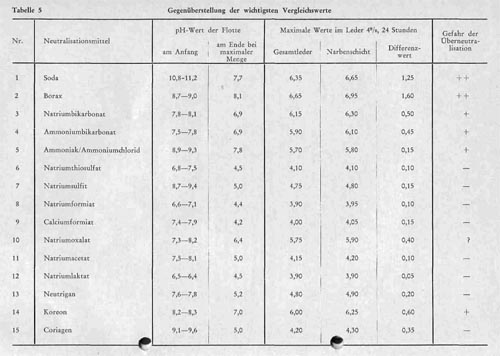
Bei der Bewertung der vorliegenden Zahlen muss natürlich berücksichtigt werden, dass sich bei den von uns durchgeführten Versuchen die Unterschiede zwischen den verschiedenen Neutralisationsmitteln bei einem so kräftigen Hautmaterial verhältnismäßig extrem auswirken. Es ist durchaus möglich, dass mit einigen Neutralisationsmitteln der Gruppe 2 bei dünnerem Hautmaterial noch etwas höhere Werte der Neutralisation erreicht werden können, und ebenso ist bei dünnerem Hautmaterial eine Gleichgewichtseinstellung viel rascher zu erreichen. Gerade die Besonderheiten eines kräftigen Hautmaterials lassen aber die Unterschiede, die sich in der Wirkung der verschiedenen Neutralisationsmittel ergeben, besonders deutlich erkennen. Um diesen Vergleich zu erleichtern, haben wir in Tabelle 5 noch einmal für die einzelnen Neutralisationsmittel die Werte zusammengestellt, die für die Beurteilung der maximal erreichbaren Neutralisation, der Gefahr einer Überneutralisation bei zu großen Mengen und der Tiefenwirkung der Neutralisation und damit der schichtmäßigen Unterschiedlichkeiten maßgebend sind. Auf Grund dieser Werte, die dem Praktiker eine Übersicht an die Hand geben, nach der für jeden Verwendungszweck die jeweils zweckmäßigsten Neutralisationsmittel ausgewählt werden können, kann über die Veränderung der Aziditätsverhältnisse von Chromleder bei der Einwirkung der verschiedenen Neutralisationsmittel zusammenfassend folgendes festgestellt werden:
Tabelle 5:
- Der pH-Wert des wässerigen Auszugs sachgemäß neutralisierter Chromleder liegt zwischen 3,5 und 5,5. Bei Werten unter 3,5 sind nach unseren früheren Untersuchungen Säureschädigungen des Leders, Metallkorrosionen, Zerstörung von Nähfäden und Ekzembildung bei Berührung mit der menschlichen Haut zu befürchten. Bei pH-Werten über 5,5 ist mit einer Überneutralisation zu rechnen, die sich in vergröbertem Narben, verminderter Festnarbigkeit namentlich in den Abfällen und im Extremfall in Entgerbung und Narbenbrüchigkeit auswirkt. Bei den meisten Ledern ist heute sogar ein pH-Wert über 5,0 unerwünscht. Der pH-Wert von 5,5 sollte auch in den Außenschichten nicht überschritten werden. Damit ist der pH-Bereich umrissen, der im Chromleder für eine sachgemäße Neutralisation zur Verfügung steht.
- Eine Gruppe von Neutralisationsmitteln, zu denen wir Soda, Borax, Natrium- und Ammoniumbikarbonat, das Ammoniak-Ammonium-Puffergemisch und auch Koreon rechnen, vermag eine kräftige Neutralisation zu bewirken, womit aber mit höherem Mengeneinsatz zugleich auch die Gefahr einer Überneutralisation verbunden ist, zumal die Tiefenwirkung der Produkte dieser Gruppe im Vergleich zu den Mitteln der zweiten Gruppe relativ schlecht ist, und die Differenzwerte zwischen 0,45 und 1,60 schwanken, so dass die pH-Werte der Narbenschicht noch höher liegen, als der bei der Lederanalyse normalerweise bestimmte pH-Wert des Gesamtleders erkennen lässt. Das gilt in erster Linie für Soda, bei der der pH-Wert der Neutralisationsflotte zu Beginn bei 10,8 - 11,2 liegt, und auch am Ende noch bei 6 - 7 bzw. bei höheren Mengen noch bei 7 - 8 liegt. Das erklärt die ausgesprochene Oberflächenneutralisation und die bei höherem Einsatz ausgeprägte Gefahr einer Überneutralisation, während andererseits die Differenzwerte, die je nach dem Mengeneinsatz zwischen 0,80 und 1,25 schwanken, zeigen, dass die Tiefenwirkung sehr ungünstig ist und sich mit zunehmender Menge, aber auch mit verlängerter Einwirkungsdauer eher verschlechtert als verbessert. Die Wirkung der Soda ist also durch eine starke Oberflächenneutralisation, die auch bei verlängerter Einwirkungsdauer bestehen bleibt, und die Gefahr einer Überneutralisation der Außenzonen bei relativ sauren Innenzonen gekennzeichnet. Ähnliches gilt für die Verwendung von Borax. Zwar liegt hier der Anfangs-pH-Wert der Lösung bei 8,7 - 9,0, also nicht so hoch wie bei Soda, der End-pH-Wert bei höheren Einsätzen aber in ähnlicher Höhe. Die dem Borax nachgerühmte milde Wirkung trifft daher nur für die Anfangsstadien zu, wenn mit geringer Menge und kurzer Einwirkungsdauer gearbeitet und nur eine ausgesprochene Oberflächenneutralisation angestrebt wird. Bei höherem Mengeneinsatz liegt dagegen der pH-Wert der Außenschichten der Leder noch höher als bei äquivalenter Sodamenge, die Gefahr der Überneutralisation mit allen damit zusammenhängenden Nachteilen ist noch verstärkt und der Differenzwert steigt bis 1,60 an, die Tiefenwirkung ist also ebenfalls schlechter als bei Soda. Natrium- und Ammoniumbikarbonat wirken graduell milder als die beiden erstgenannten Produkte. Der Anfangs-pH-Wert der Neutralisationsflotten liegt bei 7,5 - 8 und sinkt während der Neutralisation auf pH 6 - 7 ab. Sie wirken zwar auch relativ langsam, führen aber, wenn Mengen von 1 - 2% verwendet werden, und die Einwirkungsdauer nicht zu sehr ausgedehnt wird, nicht zu einer Überneutralisation, wenn auch die Gefahr der Überneutralisation, wie die erhaltenen Leder-pH-Werte zeigen, bei höheren Mengen und verlängerter Einwirkungsdauer nicht ausgeschlossen ist. Die Differenzwerte von 0,45 - 0,60 zeigen, dass die Tiefenwirkung wesentlich besser als bei den beiden erstgenannten Produkten ist, aber die Gleichmäßigkeit der Neutralisation, die die Mittel der zweiten Gruppe gewährleisten, bei weitem nicht erreicht wird. Ein ähnliches Verhalten wie die Bikarbonate zeigt auch Koreon.
- Eine gewisse Ausnahmestellung nimmt in der ersten Gruppe das Ammoniak-Ammonsalz-Puffergemisch ein. Zwar liegt der Anfangs-pH-Wert der Neutralisationsflotte mit 8,9 - 9,3 auch relativ hoch, doch sinkt der pH-Wert während der Neutralisation stärker ab, und die pH-Werte der Leder zeigen, dass die Gefahr einer Uberneutralisation gegenüber den anderen Mitteln der ersten Gruppe weiter abgeschwächt ist, wenn wir auch der in der Fachliteratur bisweilen zu findenden Angabe, ein Ammoniak Überschuss sei völlig ungefährlich, nicht zustimmen. Vor allem aber liegen die Differenzwerte mit 0,10 - 0,25 im Bereich der zweiten Gruppe, es wird eine sehr gleichmäßige Durchneutralisation erreicht. Das Puffergemisch ist daher in Übereinstimmung mit vielen praktischen Erfahrungen insbesondere dort zu empfehlen, wo eine intensivere Neutralisation angestrebt wird, die die Mittel der zweiten Gruppe nicht zu erreichen gestatten, andererseits aber eine besondere Tiefenwirkung gewünscht wird, die die anderen Mittel der ersten Gruppen nicht besitzen, wenn nicht gleichzeitig die Gefahr einer Überneutralisation der Außenschichten in Kauf genommen werden soll.
- Die zweite Gruppe der Neutralisationsmittel, zu der wir Calcium- und Natriumformiat, Natriumsulfit, Natriumacetat, Natriumlaktat, Neutrigan und Coriagen rechnen, sind als ausgesprochen milde Mittel anzusprechen. Sie zeigen zwar gewisse graduelle Unterschiedlichkeiten, führen aber sämtlich unabhängig von der angewandten Menge zu einer sehr raschen und gleichmäßigen Durchneutralisation, die Differenzwerte liegen in keinem Falle über 0,25. Die Anfangs-pH-Werte der Neutralisationsflotten liegen etwa im neutralen bzw. schwach alkalischen Bereich und sinken während der Neutralisation rasch auf etwa 4-5 ab und der maximal erreichte pH-Wert der Leder liegt auch bei höchstem Einsatz sowohl im Gesamtleder als auch in der Narbenschicht nicht über 4,5, so dass selbst bei starker Überdosierung nicht mit der Gefahr einer Überneutralisation zu rechnen ist. Lediglich bei Sulfit und Neutrigan liegen die pH-Werte der Leder bei hohem Einsatz etwas höher als bei den anderen Produkten dieser Gruppe, aber auch bei ihnen ist nicht mit der Gefahr einer Überneutralisation zu rechnen. Sämtliche Mittel dieser Gruppe wirken also ausgesprochen narbenschonend, wobei allerdings in Kauf genommen werden muss, dass eine besonders weitgehende Neutralisation mit diesen Produkten nicht erreicht werden kann. Wo für gewisse Lederarten, z. B. bei manchen technischen Ledern, höhere Entsäuerungsgrade angestrebt werden, ist entweder das Ammoniak-Ammonsalz-Puffergemisch vorzuziehen oder es sind geeignete Kombinationen zu verwenden (siehe unter.
- Natriumoxalat ist insofern keiner der beiden Gruppen zuzuordnen, als es bei kurzer Einwirkungsdauer etwa den Mitteln der zweiten Gruppe entspricht (Differenzwert 0,25), bei höheren Mengen und längerer Einwirkungsdauer dagegen eine stärkere Neutralisation als die anderen Mittel dieser Gruppe zu erreichen gestattet und auch höhere Differenzwerte von 0,4-0,5 ergibt.
- Spahrkäs hat bereits darauf hingewiesen, dass durch geeignete Kombinationen verschiedener Neutralisationsmittel besondere Neutralisationswirkungen erreicht werden können. Das gilt insbesondere für eine Vorneutralisation mit Mitteln der zweiten Gruppe und einem mengenmäßig geringeren Nachsatz mit Mitteln der ersten Gruppe, wodurch die Innenzone stärker neutralisiert und doch der Narben geschont wird und damit gleichmäßigere Säureverteilung, besserer Griff und milderer Narben erreicht wird.
- Der Auffassung, dass Natriumthiosulfat nicht zu einer nennenswerten Neutralisationswirkung fähig sei, kann nicht zugestimmt werden. Wenn ein erheblicher Überschuss angewandt wird, kann ein Neutralisationsverhalten festgestellt werden, das demjenigen der Mittel der zweiten Gruppe voll entspricht. Allerdings werden so hohe Mengen, wie wir sie verwendeten, in der Praxis nicht in Frage kommen, wohl aber Mengen von 5-8%, bei denen auch ein 4-5facher Überschuss über dem theoretischen Äquivalent vorliegt und damit neben der bekannten Bleichwirkung auch eine gewisse Neutralisation mit guter Tiefenwirkung erwartet werden kann.
Auf Grund des stark unterschiedlichen Verhaltens der verschiedenen Neutralisationsmittel hinsichtlich Intensität und Tiefenwirkung der Neutralisation ist auch ein unterschiedlicher Einfluss auf die Ledereigenschaften zu erwarten. Dabei kommt bei einer Reihe von Mitteln neben der Aziditätsbeeinflussung der Leder noch eine mehr oder weniger ausgeprägte Beeinflussung der Chromkomplexe je nach der Komplexaffinität der Anionen der Neutralisationsmittel hinzu, die vom eigentlichen Neutralisationsvorgang nicht zu trennen ist. Über entsprechende Untersuchungen zu der Frage, wie die verschiedenen Neutralisationsmittel die Ledereigenschaften beeinflussen, werden wir in Kürze berichten.
Wir danken dem Wirtschaftsministerium des Landes Baden-Württemberg für die finanzielle Unterstützung dieser Arbeit.
Literatur
- 2. Mitteilung: H. Herfeld, I. Steinlein und G. Königfeld, Welche Mindestintensitä't der Neutralisation ist bei Chromleder erforderlich? Gerbereiwissenschaft und -praxis, November 1962.
- H. Spahrkäs, Das Leder 9, 169 (1958). Siehe dort auch Hinweise auf ältere Veröffentlichungen über den Neutralisationsprozess.
- E. Stiasny und F. Prakke, Coli. 1933, 465.
Kategorien:
Quellenangabe:
Zitierpflicht und Verwendung / kommerzielle Nutzung
Bei der Verwendung von Inhalten aus Lederpedia.de besteht eine Zitierpflicht gemäß Lizenz CC Attribution-Share Alike 4.0 International. Informationen dazu finden Sie hier Zitierpflicht bei Verwendung von Inhalten aus Lederpedia.de. Für die kommerzielle Nutzung von Inhalten aus Lederpedia.de muss zuvor eine schriftliche Zustimmung (Anfrage via Kontaktformular) zwingend erfolgen.
www.Lederpedia.de - Lederpedia - Lederwiki - Lederlexikon
Eine freie Enzyklopädie und Informationsseite über Leder, Ledertechnik, Lederbegriffe, Lederpflege, Lederreinigung, Lederverarbeitung, Lederherstellung und Ledertechnologie